导读: 酸、碱、盐的组成酸是由氢元素和酸根组成的。以下是中国招生考试网www chinazhaokao com 分享的初中化学酸碱盐知识点总结,希望能帮助 ...
初中化学酸碱盐知识点总结
一、概念:
1、 酸的组成——氢离子+酸根离子
2、 碱的组成——金属离子+氢氧根离子
3、 盐的组成——金属离子+酸根离子
4、 复分解反应——由两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应。AB+CD=AD+CB
5、 稀释浓硫酸的方法——一定要把浓硫酸沿着器壁慢慢地注入水里,并不断搅动,使产生的热量迅速地扩散,切不可把水倒入浓硫酸里。
6、 中和反应——酸跟碱作用生成盐和水的反应叫做中和反应。
二、熟记常见元素和原子团的化合价口诀:
(正价)一氢钾钠银,二钙镁钡锌,三铝、四硅、五氮磷。
(负价)负一价:氟、氯、溴、碘;
负二价:氧和硫。
(可变正价):一二铜汞,二三铁,二四碳,四六硫。
(原子团的化合价
负一价:氢氧根(OH),硝酸根(NO3),氯酸根(ClO3),高锰酸根(MnO4);
负二价:硫酸根(SO4),碳酸根(CO3),亚硫酸根(SO3),锰酸根(MnO4);
负三价:磷酸根(PO4);
正一价:铵根(NH4)。
三、熟记下列反应方程式:
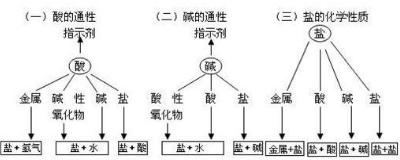
(一)酸的性质(1)与指示剂反应 紫色石蕊试液变红色,无色酚酞试液不变色。
(2)酸 + 碱 = 盐 + 水。
(3)酸 + 某些金属氧化物 = 盐 + 水。
(4)酸 + 活泼金属 = 盐 + 氢气。
(5)酸 + 盐 = 新盐 + 新酸。
1、 锌跟稀盐酸反应: Zn + 2HCl = ZnCl2 + H2 ↑ 有气泡产生,锌粒逐渐减少。
2、 锌跟稀硫酸反应: Zn + H2SO4 = ZnSO4 + H2 ↑
3、 铁跟稀盐酸反应: Fe + 2HCl = FeCl2 + H2 ↑ 有气泡产生,铁逐渐减少,
4、 铁跟稀硫酸反应: Fe + H2SO4 =FeSO4 + H2 ↑ 溶液变成浅绿色。
5、 铁锈跟稀盐酸反应:Fe2O3 +6HCl = 2FeCl3 + 3H2O 红色铁锈逐渐消失,
6、 铁锈跟稀硫酸反应:Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O 溶液变成黄色
7、 氧化铜跟稀盐酸反应:CuO + 2HCl =CuCl2 +H2O 黑色氧化铜逐渐消失,
8、 氧化铜跟稀硫酸反应:CuO + H2SO4 = CuSO4 + H2O 溶液变成蓝色。
(二)碱的性质:(1)碱溶液能使紫色石蕊试液变蓝色,无色酚酞试液变红色。
(2)碱 + 多数非金属氧化物 = 盐 + 水
(3)碱 + 酸 = 盐 + 水
(4)碱+某些盐 = 另一种盐 + 另一种碱
1、 氢氧化钠跟二氧化碳反应:2NaOH + CO2 = Na2CO3 + H2O
2、 氢氧化钠跟二氧化硫反应:2NaOH + SO2 = Na2SO3 + H2O
3、 氢氧化钠跟三氧化硫反应:2NaOH + SO3 = Na2SO4 + H2O
4、 氢氧化钙跟二氧化碳反应:Ca(OH)2 + CO2 = CaCO3↓ + H2O 使澄清石灰水变浑浊
5、 氢氧化钠跟稀硫酸反应:2NaOH + H2SO4 = Na2SO4 + 2H2O
6、 氢氧化钠跟稀盐酸反应:NaOH + HCl = NaCl + H2O
7、 生石灰跟水反应:CaO + H2O =Ca(OH)2
(三)盐的性质:(1)盐 + 某些金属=另一种盐 + 另一种金属。
(2)盐 + 某些酸 = 另一种盐 + 另一种酸。
(3)盐 + 某些碱 = 另一种盐 + 另一种碱
(4)盐 + 某些盐 = 另一种盐 + 另一种盐
1、 硫酸铜溶液跟铁反应:CuSO4 + Fe = ZnSO4 +Fe 铁表面覆盖红色物质,溶液由蓝色变浅绿色
2、 碳酸钠跟盐酸反应:Na2CO3 + 2HCl = 2NaCl +H2O +CO2↑有气泡产生固体逐渐减少
3、 碳酸氢钠跟盐酸反应:NaHCO3 + HCl = NaCl +H2O + CO2↑有气泡产生固体逐渐减少
4、 石灰石跟稀盐酸反应:CaCO3 + 2HCl = CaCl2 +H2O +CO2↑有气泡产生固体逐渐减少
5、 硝酸银跟稀盐酸反应:AgNO3 + HCl = AgCl↓ +HNO3 有白色沉淀产生
6、 氯化钡跟稀硫酸反应:BaCl2 + H2SO4 = BaSO4↓ + 2HCl 有白色沉淀产生
7、 氢氧化钙根碳酸钠溶液反应:Ca(OH)2 + Na2CO3 = 2NaOH + CaCO3↓ 有白色沉淀产生
8、 硝酸银溶液跟氢氧化钠溶液反应:AgNO3 + NaCl = AgCl↓ + NaNO3有白色沉淀产生
9、 氯化钡溶液跟硫酸钠溶液反应:BaCl2 + Na2SO4 = 2NaCl + BaSO4↓有白色沉淀产生
四、金属活动性顺序表:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
五、溶解性表:
(1) 大多数酸可溶(HCl、HNO3、H2CO3有挥发性、浓H2SO4有吸水性。)
(2) 碱的溶解性:钾、钠、钡、铵溶、钙微溶,其余碱 全不溶。
(3) 盐的溶解性:
钾、钠、铵、硝四盐溶。
氯化物除AgCl不溶外,其余全溶。
硫酸盐除BaSO4不溶,Ag2SO4、CaSO4微溶外,其余全溶。
碳酸盐除钾、钠、铵盐全溶、MgCO3微外,其余全不溶。
六、反应条件:
1、 复分解反应的条件——生成物中有沉淀析出,或有气体放出,或有水生成
2、 金属跟酸反应的条件——
(1) 在金属活动性顺序表中,金属要排在氢前。
(2) 浓硫酸、硝酸跟金属反应不能生成氢气。
(3) 铁发生置换反应时,生成+2价的铁的化合物。
3、 金属跟盐反应的条件——
(1)在金属活动性顺序表中,单质的金属要比盐中金属活泼。
(2)反应物中的盐要可溶。
(3)K、Ca、Na、Ba等金属跟盐反应不能生成另一种盐和另一种金属。
4、 盐跟盐反应的条件——反应物都要可溶,生成物要有沉淀。
5、 盐跟碱反应的条件——反应物都要可溶,生成物要有沉淀或气体。
七、熟记常见物质的俗称和化学式:
生石灰—— CaO 熟石灰——Ca(OH)2 石灰石、大理石—— CaCO3
食盐——NaCl 火碱、烧碱、苛性钠—— NaOH 纯碱、苏打——Na2CO3
小苏打—— NaHCO3 铁锈、赤铁矿——Fe2O3 赤铁矿—— Fe3O4
金刚石、石墨—— C 干冰——CO2 冰—— H2O
天然气(甲烷)——CH4 酒精(乙醇)—— C2H5OH 醋酸(乙酸)——CH3COOH
八、熟记常见物质的颜色:
红色的固体——Cu、Fe2O3 、P(红磷)
黑色的固体——C、CuO、Fe3O4、FeO、MnO2
白色的固体——KClO3、P2O5、P(白磷)、CuSO4(无水硫酸铜)、KCl、NaCl等
暗紫色的固体——KMnO4 黄色的固体—— S
蓝色的固体——CuSO4?5H2O 蓝色絮状沉淀——Cu(OH)2
红褐色絮状沉淀——Fe(OH)3 常见不溶于酸的白色沉淀——BaSO4、AgCl
溶于酸并放出使澄清石灰水变浑浊的气体的白色沉淀——BaCO3、CaCO3等不溶性碳酸盐的沉淀
溶于酸但不产生气体的白色沉淀——Mg(OH)2、Al(OH)3等不溶性碱的沉淀
蓝色的溶液—— CuSO4、CuCl2、Cu(NO3)2等含Cu2+溶液
浅绿色的溶液——FeSO4、FeCl2等含Fe2+溶液
黄色的溶液——FeCl3、Fe2(SO4)3、Fe(NO3)3等含Fe3+溶液
九、物质的检验和鉴别:
1、 检验稀盐酸(或Cl-)——取少量待检液体于洁净的试管中,滴入几滴AgNO3溶液和稀HNO3,有白色沉淀产生。
2、 检验稀硫酸(或SO42-)——取少量待检液体于洁净的试管中,滴入几滴BaCl2溶液和稀HNO3,有白色沉淀产生。
3、 检验CO32-——取少量待检液体于洁净的试管中,滴入几滴稀HCl,有使澄清石灰水变浑浊的气体产生。
4、 检验NH4+——取少量待检物于洁净的试管中,滴入适量NaOH溶液并加热,有使湿的红色石蕊试纸变成蓝色的气体产生。
5、 鉴别稀盐酸和稀硫酸——分别取少量待检液体于两支洁净的试管中,各滴入几滴BaCl2溶液,有白色沉淀产生的原溶液是稀硫酸,无现象产生的原溶液是稀盐酸。
6、 鉴别Ca(OH)2和NaOH溶液——分别取少量待检液体于两支洁净的试管中,分别通入CO2气体(或各滴入几滴Na2CO3溶液),有白色沉淀产生的原溶液是Ca(OH)2,无现象产生的原溶液是NaOH。
◎补充下列反应方程式:
1、 氢氧化铜跟稀盐酸反应: Cu(OH)2 + 2HCl = CuCl2 + 2H2O 蓝色沉淀消失
2、 氢氧化铜跟稀硫酸反应: Cu(OH)2 + H2SO4 = CuSO4 + 2H2O 变成蓝色溶液
3、 氢氧化钠跟硫酸铜溶液反应:2NaOH + CuSO4 = Na2SO4 + Cu(OH)2 ↓ 有蓝色沉淀产生
4、 氢氧化钠跟氯化铁溶液反应:3NaOH + FeCl3 = Fe(OH)3↓ +3NaCl 有红褐色沉淀产生
◎判断溶液的酸碱性——用指示剂,溶液的酸碱度——用pH来表示。
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14
中性 ← 酸性增强 碱性增强 →
紫色石蕊 无色酚酞
pH<7为酸性 显红色 显无色
pH=7为中性 显紫色 显红色
pH>7为碱性 显蓝色 显红色
◎干燥剂的选择:
1、浓硫酸可干燥:酸性气体(如:CO2、SO2、SO3、NO2、HCl、)
中性气体(如:H2、O2、N2、CO)
※不能干燥碱性气体(如:NH3)
2、氢氧化钠固体、生石灰、碱石灰可干燥:碱性气体(如:NH3)
中性气体(如:H2、O2、N2、CO)
※不能干燥酸性气体(如:CO2、SO2、SO3、NO2、HCl、)
3、无水硫酸铜固体遇水由白色变蓝色,可检验水的存在,并吸收水蒸气。
一些知识点
单质:非惰性气体一般由两个原子组成: F2,O2,H2,Cl2
惰性气体一般由一个原子组成:He,Ne,Ar,Kr,Xe
化合物: 氢化物居多:H2S,HCl,H3P,HF,HBr,HI
初中化学酸碱盐知识点总结相关热词搜索:知识点 酸碱 初中
1、 量筒是粗量器,对其最小刻度、起始刻度、准确度、读数及选取等,笔者总结为:起始刻度为量程的1 10;最小刻度 高中化学知识点归纳:量筒篇。(2015-08-01)
2、 晶体具有规则的几何外形、固定的熔沸点、各向异性(如云母的解离性各个方向不同)。其原因是组成晶体的质点( 化学知识点解析:晶体篇。(2015-08-01)
3、知识点 离子 化学1)有气体产生。如CO32-、SO32-、S2-、HCO3-、HSO3-、HS-等易挥发的弱酸的酸根与H+不能大量共存。高考化学知识点大全:离子共存问题。(2015-11-06)
4、 "有机化学"知识模块 1 羟基官能团可能发生反应类型:取代、消去、酯化、氧化、缩聚、中和反应 正确,取代(醇、酚、羧酸);消去 高中化学知识点总结。(2016-03-10)
5、高考复习一轮化学知识点解读(共5篇)高三有机化学一轮复习知识点归纳专题一 官能团与有机物类别、性质的关系【考纲解读】:有机化学是高中化学的主干知识,是高考化学中必考内容之一,学习有机化学就是学习官能团,考纲中对官能团的要求是:掌握官能团的名称和结构,了解官能团在化合物中的作用,掌握个主要官能团的性质和主要化学反应,并能结合同系物的高考复习一轮化学知识点解读。(2016-07-29)
6、高二化学知识点(共9篇)高二化学知识点总结(精)化学有机基础知识点总结 精品1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。高二化学知识点。(2016-11-11)
7、 高中化学知识点总结 化学反应方程式,是用化学式表示化学反应的式子。化学方程式反映的是客观事实。下面是www chinazhaokao com中国 高中化学知识点总结大全。(2016-12-08)
8、高二化学知识点总结(共9篇)高二化学知识点总结(精)化学有机基础知识点总结 精品1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。高二化学知识点总结。(2016-12-22)
9、 化学(英语:Chemistry)是一门研究物质的性质、组成、结构、变化、用途、制法,以及物质变化规律的自然科学。化学与工业、农业、日常生 九年级上册化学知识点。(2017-02-13)
最新推荐成考报名
更多- 歇后语_歇后语大全_歇后语大全及答案_爆笑歇后语
- 大学排名_大学排名2018排行_大学查询_中国大学名单
- 成语大全_四字成语_在线成语词典_成语查询
- 成语接龙大全查询,成语接龙游戏,在线成语接龙
- 全国安全教育平台入口_学校安全教育平台
- 社保查询网-社会保障卡查询,社会保险查询,社保网上查询
- 汉字简体繁体转换_在线繁体字转换工具
- 数字大写转换|人民币金额(数字)大小写转换在线工具
- 年龄计算器实际岁数计算器 - 周岁虚岁计算器
- 产假计算器-算产假计算器在线2018-2018年产假自动计算器
- 预产期计算器-怀孕孕期计算器-怀孕天数计算
- 中国文库网-教育资源网-范文文章
- 邮编区号查询网
- 致富商机网-致富点子_创业项目
- 创业项目网--最热门的投资项目
- 中国邮政邮编查询号码
- 电话区号查询
- 全国车牌号归属地大全
- 在线网速测试|宽带速度测试
- 人民币汇率查询
- ●理财有没有风险 金融互联网理财
- ●qq网名
- ●2016最新伤感说说
- ●谈笑风生造句
- ●读书的名言
- ●资产清查报告
- ●贫困户申请书
- ●财务自查报告
- ●离婚起诉书
- ●赞美老师的演讲稿
- ●车间管理
- ●车辆购置税
- ●跨越百年的美丽读后感
- ●跟女友离别的话
- ●超市管理制度
- ●起诉状范本
- ●赠别诗大全
- ●描写夏天的句子
- ●描写友谊的诗句
- ●迁户口申请书
- ●转正申请表范本
- ●这个杀手不太冷台词
- ●运动会稿子精选
- ●那么那么造句
- ●送给男朋友的情话大全
- ●钳工实训报告
- ●霸气说说大全
- ●骂人不带脏字的
- ●幼儿园见习个人总结
- ●追女孩子的短信

